Механизмы образования АФК, влияние питания и функции пероксисом
Оксидативный стресс — это состояние, при котором в клетке накапливается избыточное количество активных форм кислорода (АФК). К реактивным формам кислорода относятся супероксид (O₂⁻•), перекись водорода (H₂O₂), гидроксильный радикал (•OH). Опасные радикалы обозначаются как H·, OH· — у них есть неспаренный электрон; безопасные формы — H⁺, OH⁻, не имеют неспаренных электронов.
Источник проблемы
АФК образуются всегда — это нормальная часть дыхательной цепи. Стресс возникает, когда их образование выходит из-под контроля. Примеры таких ситуаций:
·Гипоксия-реоксигенация (затекшая нога, интенсивная физическая нагрузка, апноэ, ныряние)
·Воспаление
·Воздействие токсинов и радиации
·Митохондриальная дисфункция
Цикл Кребса (цикл лимонной кислоты)
Основная задача цикла Кребса — полное окисление ацетил-КоА до CO₂, запасание энергии в виде NADH и FADH₂, передача этой энергии в дыхательную цепь, где образуется основная масса АТФ. NADH и FADH₂ являются источником электронов для цепи переноса электронов. Цепь состоит из 4 комплексов (I, II, III, IV) и 2 мобильных переносчиков (коэнзим Q и цитохром С).
Образование активных форм кислорода
В норме в митохондриях около 0,25–3% электронов, проходящих через электронно-транспортную цепь (ЭТЦ), не достигают конечного акцептора — комплекса IV, где из кислорода образуется вода. Некоторые электроны «утекают» и напрямую восстанавливают молекулярный кислород, в результате чего образуется супероксид-анион-радикал — первичная активная форма кислорода.
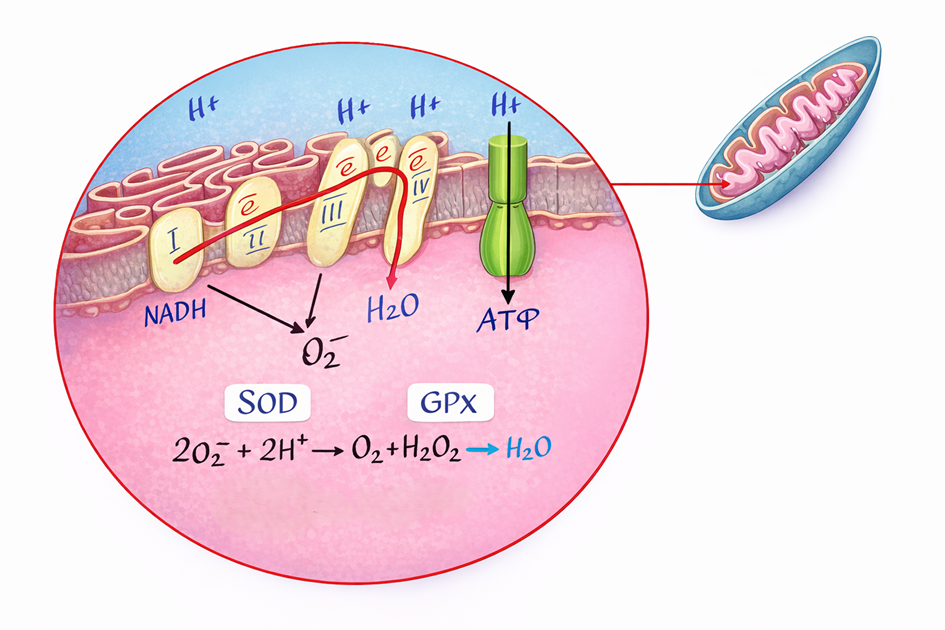
Основные места утечки электронов — комплекс I (NADH-дегидрогеназа) и комплекс III (цитохром-bc1). Образовавшийся супероксид быстро нейтрализуется ферментами супероксиддисмутазами (SOD), превращаясь в перекись водорода, которая затем обезвреживается глутатионпероксидазой (GPX).
Как уже упоминалось, в норме в митохондриях образуется около 0,25–3% электронов АФК. Они выполняют сигнальную функцию: регулируют работу митохондрий, аутофагии и синтез антиоксидантных ферментов.
Активные формы кислорода — двойная роль
·Польза: В малых дозах АФК помогают клетке адаптироваться, управляют митохондриями, запускают очистку (аутофагия, митофагия), активируют защитные гены (Nrf2), регулируют обмен веществ. Небольшой уровень АФК — «сигнальный маячок», помогающий клетке гибко реагировать на изменения.
·Вред: Если АФК больше, чем клетка может обезвредить, начинается окислительный стресс:
·Повреждение ДНК — одно- и двуцепочечные разрывы, мутации
·Разрушение липидов мембран — оболочки клеток и органелл становятся нестабильными
·Порча белков — потеря формы, слипание
·Страдают митохондрии — падает мембранный потенциал, нарушается работа дыхательной цепи
В конечном итоге клетка либо аккуратно погибает (апоптоз), либо разрушается с воспалением (некроз) — в зависимости от масштаба повреждения.
Кратко
·Мало АФК — это сигнал и польза, инструмент регулировки работы клетки.
·Много АФК — повреждение на всех уровнях: ДНК, белки, липиды, митохондрии.
·Баланс между этими состояниями определяет, будет ли АФК «хорошим помощником» или «опасным разрушителем».
Калорийное ограничение: влияние на окислительный стресс
Калорийное ограничение (CR, calorie restriction) снижает базовый уровень АФК и делает клетку более устойчивой к окислительному стрессу. Это происходит за счёт:
1.Прямой эффект: уменьшение поступающей энергии снижает объём субстратов для «сжигания» в митохондриях, уменьшается интенсивность образования АФК.
2.Косвенный эффект (гормезис): CR вызывает мягкий метаболический стресс, запускает адаптационные программы:
3.Активируется экспрессия генов антиоксидантных белков
4.Усиливаются аутофагия и митофагия
5.Снижается хроническое воспаление
Пероксисомы — дополнительный источник АФК
Ещё одним источником АФК, особенно перекиси водорода (H₂O₂), являются пероксисомы — мембранные органеллы, многочисленные в клетках печени и почек (детоксикация), а также в клетках нервной системы (синтез липидов для миелиновых оболочек).
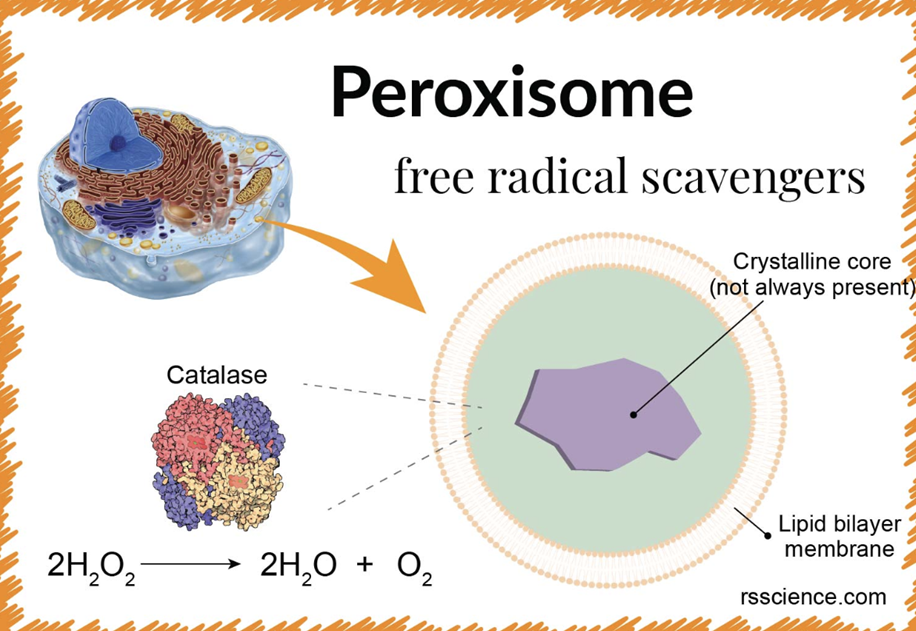
Пероксисомы содержат ферменты окисления, включая оксидазы и каталазу, выполняют широкий спектр метаболических и защитных функций. Главная функция — β-окисление жирных кислот. В митохондриях β-окисление служит для получения энергии (образование АТФ), а в пероксисомах — для укорочения и преобразования очень длинных жирных кислот.
Если пероксисомы повреждены или фермент каталаза работает плохо:
·H₂O₂ накапливается
·АФК выходят в цитозоль
·Усиливается окислительный стресс
В результате АФК повреждают клеточные структуры, включая ДНК. Повреждение ДНК активирует фермент PARP (поли-АДФ-рибозо-полимеразу), участвующий в её репарации.
Связь ограничения калорий, диеты и митохондрий
Ограничение калорий снижает поступление энергетических субстратов и увеличивает соотношение AMP/ATP. Рост AMP активирует AMPK — главный энергетический сенсор клетки. AMPK ингибирует mTOR и активирует ULK1, что запускает аутофагию. Поврежденные митохондрии удаляются через митофагию (PINK1/Parkin). Одновременно AMPK и сиртуины активируют PGC-1α, стимулируя биогенез новых митохондрий. Если повреждение клеточных структур и митохондрий слишком велико и восстановление невозможно, через p53 и митохондриальный путь запускается апоптоз.
Связь ограничения калорий, диеты и пероксисом
PPARα (Peroxisome proliferator-activated receptor alpha) — ядерный рецептор, работающий как молекулярный переключатель для генов, участвующих в метаболизме жирных кислот.
При ограничении калорий или голодании повышается уровень свободных жирных кислот в крови: организм использует жировые запасы как источник энергии. Эти жирные кислоты активируют PPARα, который включает экспрессию генов, отвечающих за β-окисление жирных кислот в митохондриях и пероксисомах.
В результате увеличивается количество пероксисом и активность ферментов, участвующих в окислении жирных кислот и детоксикации. Пероксисомальная система клетки начинает работать более эффективно, улучшая метаболизм липидов и контроль окислительных процессов.
Митохондриальный гормезис
Митохондриальный гормезис — это явление, при котором умеренный стресс митохондрий приводит к усилению защитных механизмов клетки и в долгосрочной перспективе способствует увеличению продолжительности жизни. Ключевая идея заключается в том, что небольшое количество стресса действует как сигнал для адаптации, а не как повреждение.
Когда митохондрии работают в условиях слегка повышенной нагрузки — например при ограничении калорий, физической активности, воздействии холода или периодах голодания — они начинают вырабатывать немного больше реактивных форм кислорода (ROS). При умеренном уровне эти молекулы не столько повреждают клетку, сколько выполняют роль сигнальных молекул, сообщая клетке о необходимости адаптации к изменившимся условиям.
Этот сигнал запускает несколько важных внутриклеточных регуляторных систем. Одной из них является AMPK — фермент, который выполняет роль энергетического сенсора. Он активируется при повышении отношения AMP к ATP и переводит клетку в режим экономии энергии и восстановления. AMPK стимулирует катаболические процессы, усиливает использование жирных кислот и активирует аутофагию — механизм удаления поврежденных клеточных компонентов.
Параллельно активируются сиртуины, особенно SIRT1. Эти белки зависят от уровня NAD⁺ и регулируют активность многих транскрипционных факторов посредством деацетилирования. Через такие мишени, как PGC-1α, FOXO и p53, сиртуины усиливают антиоксидантную защиту, репарацию ДНК и метаболическую адаптацию клетки.
Одновременно включается транскрипционный фактор NRF2 — главный регулятор антиоксидантной системы. Он активирует экспрессию генов ферментов, нейтрализующих реактивные формы кислорода, таких как супероксиддисмутаза, каталаза и глутатионпероксидаза. Благодаря этому клетка усиливает собственную систему защиты от окислительного повреждения.
Важную роль играют и транскрипционные факторы семейства FOXO. Они регулируют экспрессию генов, связанных с антиоксидантной защитой, аутофагией и репарацией ДНК. Их активация помогает клетке справляться со стрессом и поддерживать стабильность генома.
Одним из ключевых результатов этих сигнальных процессов становится усиление клеточной «очистки». Запускаются механизмы аутофагии и митофагии — процессов, при которых клетка удаляет поврежденные белки, агрегаты и дефектные митохондрии. Это предотвращает накопление клеточного «мусора», который со временем способствует старению.
Параллельно с удалением поврежденных органелл усиливается синтез новых митохондрий. Через сигнальный путь AMPK–SIRT1 активируется коактиватор PGC-1α, который стимулирует митохондриальный биогенез. В результате формируются новые, функционально более эффективные митохондрии.
После завершения адаптационного ответа клетка оказывается в более устойчивом состоянии. Митохондрии начинают работать эффективнее, уровень образования ROS снижается, антиоксидантные системы усиливаются, а механизмы аутофагии работают активнее. Метаболизм становится более гибким и устойчивым к стрессу.
Благодаря этому замедляются основные процессы, связанные со старением: накопление поврежденных митохондрий, образование белковых агрегатов, хроническое воспаление, метаболические нарушения и повреждение ДНК. Именно поэтому умеренный митохондриальный стресс в ряде случаев связан с увеличением продолжительности жизни.
Интересно, что этот механизм объясняет и один парадокс: в некоторых исследованиях высокие дозы антиоксидантов, например витаминов C и E, могут ослаблять полезный эффект физической нагрузки. Это происходит потому, что антиоксиданты подавляют сигнальную роль ROS, и адаптационные программы клетки активируются слабее.
Наиболее мощными естественными стимулами митохондриального гормезиса считаются регулярная физическая активность, ограничение калорий, интервальное голодание, воздействие холода и состояния, при которых организм временно переходит на использование жиров и кетоновых тел в качестве источника энергии. Все эти факторы создают умеренный энергетический стресс, который запускает адаптационные механизмы и повышает устойчивость клеток.
электронов «утекают» в митохондриях, образуя АФК — при избытке калорий это становится проблемой
0,25–3%
снижения АФК при ограничении калорий: меньше топлива и запуск адаптации (гормезис)
2 пути
защиты клетки включаются при умеренном стрессе: AMPK, сиртуины, NRF2, FOXO, аутофагия
5 систем
Другие материалы
Получить первичную оценку документов
Пришлите ваши выписки/снимки/анализы и мы вышлем вам первичную оценку ваших документов






