Висцеральный жир и его роль в возникновении и развитии метаболического синдрома
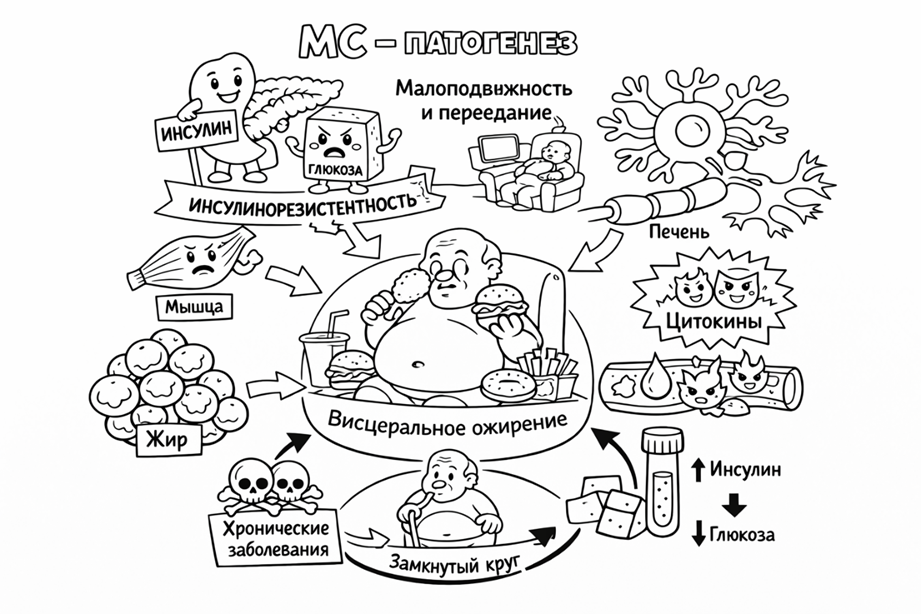
Метаболический синдром — это единый патологический процесс, в основе которого лежит инсулинорезистентность. Однако ключевым фактором, который поддерживает и усиливает этот процесс, является висцеральный жир.
🟢 Энергетический аспект метаболического синдрома
Организм человека обладает выраженной способностью к запасанию энергии.
В жировой ткани может содержаться огромный энергетический резерв:
— примерно 150 000 ккал в 20 кг жира.
В то же время запасы углеводов ограничены:
гликоген печени и мышц составляет около 2000 ккал, чего хватает примерно на сутки.
Это объясняет, почему организм активно стремится запасать энергию в виде жира и почему нарушение регуляции этого процесса приводит к накоплению висцеральной жировой ткани.
В отличие от подкожной жировой ткани, висцеральный жир, расположенный вокруг внутренних органов, обладает высокой метаболической активностью. Это не просто энергетическое депо, а полноценный эндокринный орган, который активно участвует в регуляции обмена веществ.
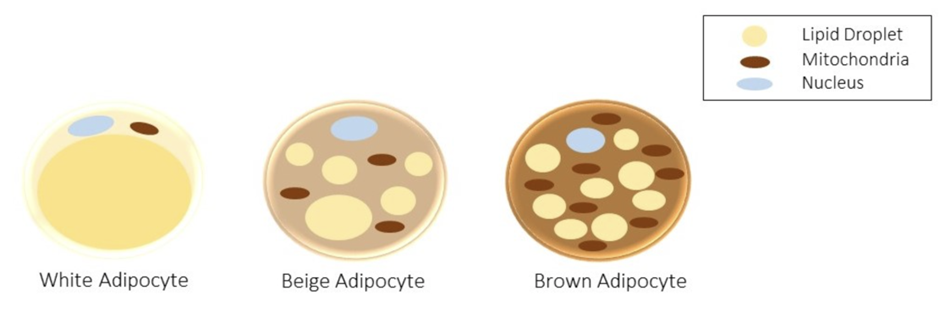
Адипоциты висцерального жира имеют ряд принципиальных особенностей. Они менее чувствительны к действию инсулина, что приводит к ослаблению его антилиполитического эффекта. В результате такие клетки легче подвергаются липолизу и активнее высвобождают свободные жирные кислоты в кровоток. Дополнительно у них выше плотность β-адренорецепторов, что делает их более чувствительными к липолитическим сигналам.
Особое значение имеет анатомическая особенность висцеральной жировой ткани: её дренаж осуществляется в систему воротной вены. Это означает, что свободные жирные кислоты и биологически активные вещества, выделяемые висцеральным жиром, поступают непосредственно в печень. Таким образом, печень оказывается под постоянным воздействием продуктов метаболизма жировой ткани.
Повышенный поток свободных жирных кислот в печень приводит к ряду изменений. Усиливается синтез триглицеридов и липопротеинов очень низкой плотности, развивается стеатоз печени, формируется атерогенная дислипидемия. Одновременно нарушается регуляция глюкозного обмена: печень продолжает вырабатывать глюкозу даже при высоком уровне инсулина, что является одним из ключевых проявлений инсулинорезистентности.
Однако влияние висцерального жира не ограничивается только поставкой свободных жирных кислот. Жировая ткань активно секретирует адипокины, цитокины и хемокины, которые формируют состояние хронического низкоуровневого воспаления.
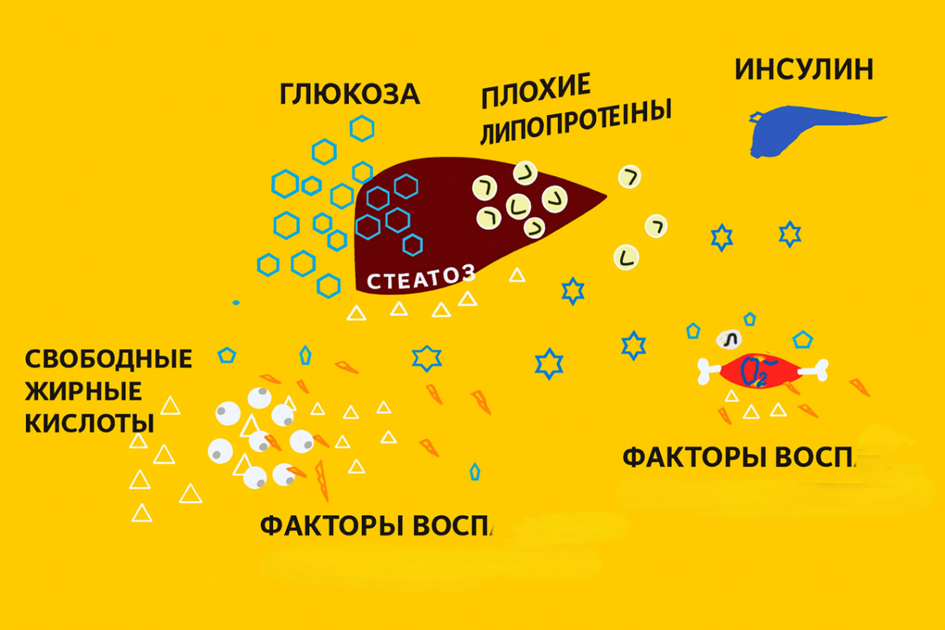
К числу провоспалительных факторов относятся TNF-α, IL-6, MCP-1 и другие медиаторы, которые нарушают передачу сигнала от инсулинового рецептора внутри клетки. Одновременно снижается уровень адипонектина — гормона, повышающего чувствительность тканей к инсулину и обладающего противовоспалительным действием. Снижение адипонектина является одним из ранних признаков висцерального ожирения.
Под действием хемокинов в жировую ткань активно привлекаются иммунные клетки, прежде всего макрофаги. Это усиливает воспаление и закрепляет патологический процесс. В результате висцеральный жир превращается в источник постоянных метаболических и воспалительных сигналов.
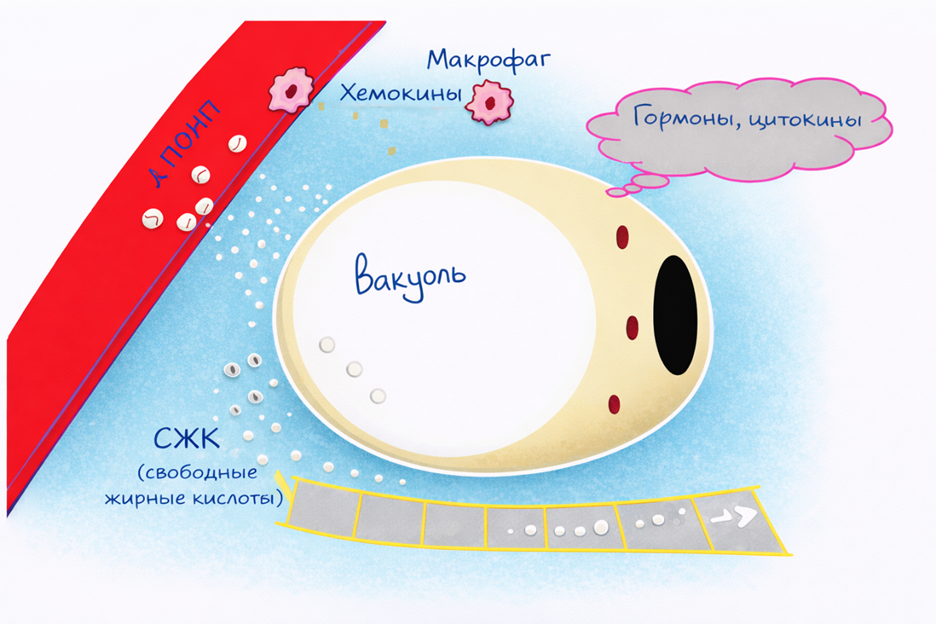
На молекулярном уровне свободные жирные кислоты и цитокины активируют внутриклеточные пути, которые нарушают нормальную работу инсулинового сигнального каскада. Это приводит к снижению активности переносчика GLUT4 в мышечной и жировой ткани и, как следствие, к ухудшению утилизации глюкозы клетками.
Скелетные мышцы, являющиеся основным потребителем глюкозы, начинают хуже её захватывать. В крови сохраняется повышенный уровень глюкозы, что стимулирует поджелудочную железу к увеличению секреции инсулина. Формируется гиперинсулинемия, которая на начальных этапах носит компенсаторный характер.
Парадокс метаболического синдрома заключается в том, что при высокой концентрации инсулина его основные эффекты реализуются неравномерно. В мышцах действие гормона ослаблено, тогда как в печени и жировой ткани его липогенные эффекты частично сохраняются. Это приводит к усилению синтеза жира и дальнейшему накоплению висцеральной жировой ткани.
🟢 Липидный профиль при метаболическом синдроме
Норма
> 1,0 (м) / > 1,2 (ж)
Часто нормальны, но увеличена доля мелких плотных частиц
Повышен
Понижен
висцеральный жир усиливает инсулинорезистентность, а инсулинорезистентность, в свою очередь, способствует дальнейшему накоплению жира.
🟢 🟪 Как висцеральный жир вызывает инсулинорезистентность
Каскад выглядит следующим образом:
- Свободные жирные кислоты (FFA), TNF-α, IL-6, IL-1β активируют рецептор TLR4.
- TLR4 запускает внутриклеточные сигнальные пути (IKKβ, JNK, PKC-θ).
- Эти ферменты изменяют фосфорилирование IRS-1 (по серину вместо тирозина).
- Нарушается передача сигнала от инсулинового рецептора.
- Не активируется путь PI3K-Akt.
- Переносчик GLUT4 не перемещается к мембране клетки.
- Глюкоза не поступает в клетку.
Дополнительное влияние висцеральный жир оказывает на сосудистую систему. Гиперинсулинемия способствует задержке натрия и воды в почках, повышает активность симпатической нервной системы и стимулирует рост гладкомышечных клеток сосудистой стенки. Провоспалительные медиаторы и оксидативный стресс повреждают эндотелий, снижается выработка оксида азота, который в норме обеспечивает расслабление сосудов.
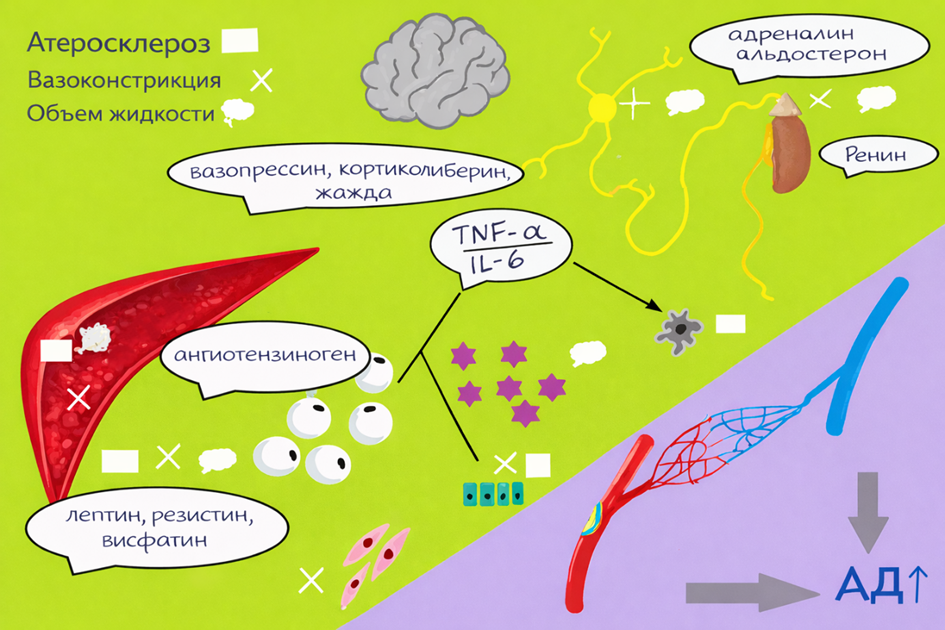
Это один из ключевых молекулярных механизмов формирования инсулинорезистентности.
Скелетные мышцы при этом теряют способность эффективно утилизировать глюкозу, что ведёт к её накоплению в крови и компенсаторному повышению уровня инсулина.
В результате сосуды становятся менее эластичными, их тонус повышается, и развивается артериальная гипертензия. Вклад в этот процесс вносит и локальная ренин-ангиотензин-альдостероновая система жировой ткани, которая усиливает сосудистый спазм и задержку жидкости.
🟢 🟩 Локальная РААС — ещё один слой воспаления
РААС (ренин–ангиотензин–альдостероновая система) — это система гормонов, регулирующая артериальное давление и водно-солевой баланс.
Висцеральная жировая ткань способна самостоятельно синтезировать компоненты этой системы:
• ангиотензиноген
• ангиотензин II
• альдостерон
Это приводит к усилению сосудистого спазма, задержке натрия и воды, воспалению и ремоделированию сосудистой стенки.
Висцеральный жир также активно выделяет провоспалительные цитокины и хемокины, формируя хроническое низкоуровневое воспаление. Эти сигналы нарушают передачу инсулинового сигнала внутри клетки.
Хроническое повышение уровня глюкозы оказывает дополнительное повреждающее действие. Глюкоза вступает в реакции гликации с белками, образуются конечные продукты гликирования, которые изменяют структуру сосудистой стенки и ухудшают микроциркуляцию. Одновременно усиливается оксидативный стресс, повреждаются клеточные структуры и активируется воспаление.
На этом фоне в сосудистой стенке происходит накопление липопротеинов низкой плотности, их окисление и поглощение макрофагами с образованием пенистых клеток. Это является основой формирования атеросклеротических бляшек.
Таким образом, висцеральный жир запускает и поддерживает сразу несколько ключевых патологических процессов: инсулинорезистентность, хроническое воспаление, нарушение липидного обмена, повреждение сосудов и повышение артериального давления.
В совокупности эти изменения приводят к развитию метаболического синдрома и его осложнений — сахарного диабета 2 типа, атеросклероза, сердечно-сосудистых заболеваний, жировой болезни печени.
Важно подчеркнуть, что метаболический синдром во многом повторяет механизмы биологического старения: хроническое воспаление, оксидативный стресс, эндотелиальная дисфункция и нарушение гормональной регуляции. Поэтому его развитие сопровождается ускоренным функциональным старением организма.
доставки жирных кислот к тканям: экзогенный (из пищи), эндогенный (из печени) и межклеточный
3 пути
липопротеинов переносят жиры в крови — от хиломикронов до ЛПВП, каждый со своей ролью
5 типов
фосфолипида — гидрофильная головка и гидрофобные хвосты — создают все клеточные мембраны
2 части
Другие материалы
Получить первичную оценку документов
Пришлите ваши выписки/снимки/анализы и мы вышлем вам первичную оценку ваших документов






