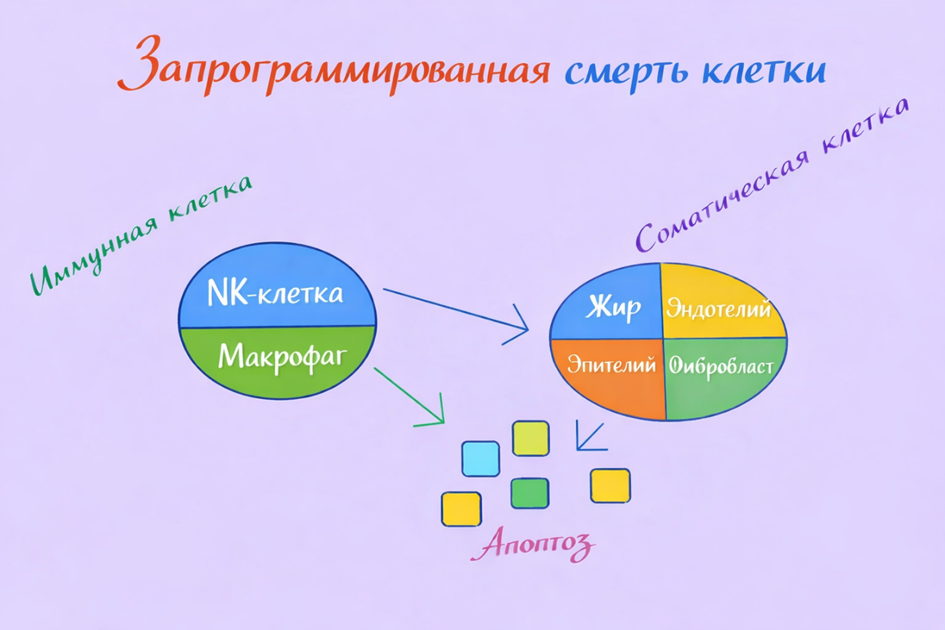
В норме внутриклеточная система работает так, что при необходимости обеспечивает своевременное удаление повреждённых клеток. Однако при старении или хроническом воспалении этот баланс нарушается: клетка перестаёт делиться, активно сигнализирует воспалением, но становится устойчивой к апоптозу. В подобном состоянии она не погибает, а превращается в долгоживущий источник воспалительных сигналов.
Причины включают разрывы ДНК, укорочение теломер, нарушения работы митохондрий, хронический окислительный стресс, накопление неправильно свернутых белков, изменение pH, а также осмотического и ионного баланса.
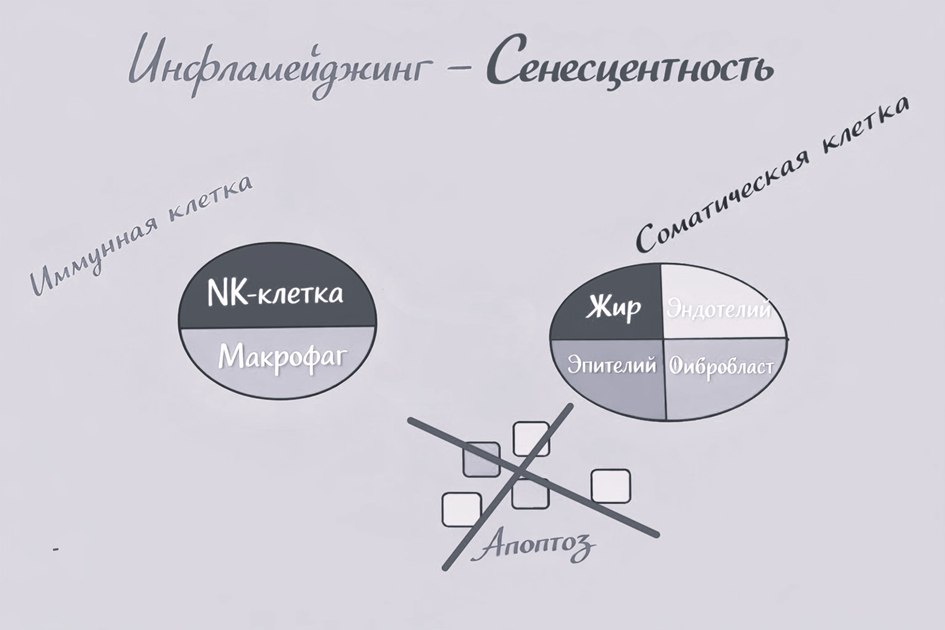
С возрастом сенесцентные клетки накапливаются, и их секреторный фенотип перестаёт быть локальным. Формируется постоянная самоподдерживающаяся сеть воспалительных сигналов, что приводит к состоянию, известному как инфламейджинг — хроническое низкоуровневое воспаление, поддерживаемое накоплением долгоживущих сенесцентных клеток и возрастными изменениями иммунной системы.
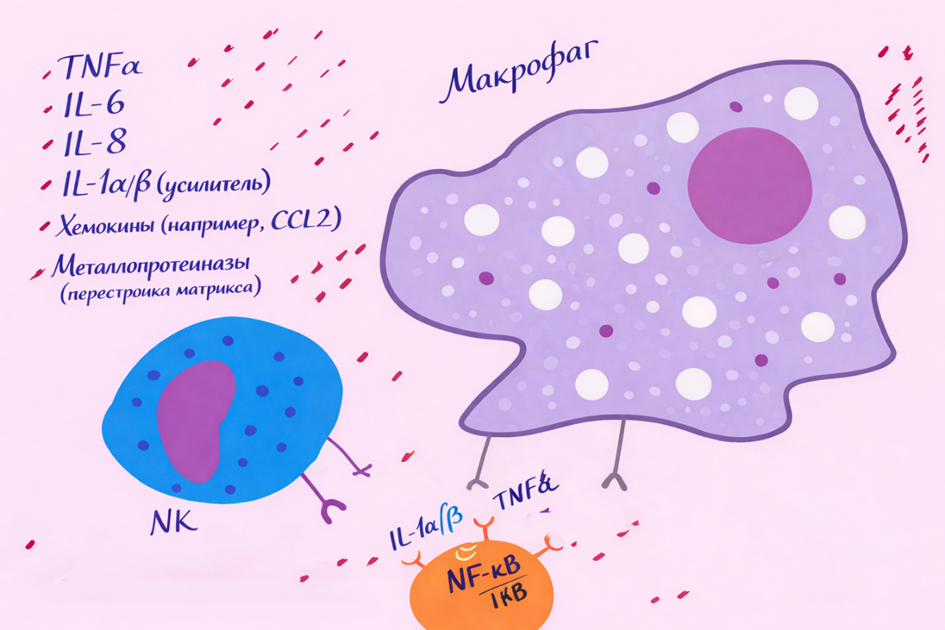
TNF-α (Tumor Necrosis Factor alpha)
Один из самых мощных провоспалительных цитокинов.
·Кем вырабатывается?
·макрофагами и моноцитами,
·Т-клетками,
·NK-клетками,
·адипоцитами,
·эндотелием.
Основные действия:
активирует NF-κB, усиливая экспрессию других цитокинов;
увеличивает проницаемость сосудов;
стимулирует приток нейтрофилов;
вызывает лихорадку;
участвует в разрушении тканей при аутоиммунных болезнях.
Хроническое воспаление формирует «воспалительный возраст» (inflammaging) — биологическое старение, отражающееся в маркёрах, таких как CXCL9, IL-6, VEGFA, PDGFA/B и других. При этом немного повышены уровни IL-6, TNF-α, CRP, IL-1β.
Внутренний контур
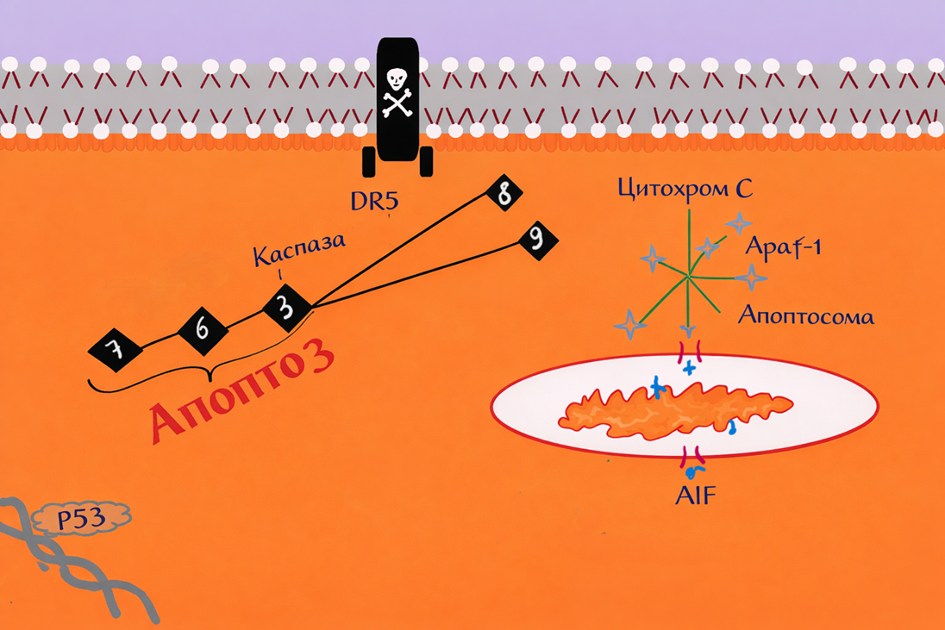
Повреждение ДНК и укорочение теломер запускают систему ответа на повреждение ДНК, в рамках которой активируется белок p53. Его уровень регулируется главным образом взаимодействием с негативным регулятором MDM2, который связывает p53 и помечает его для деградации, поддерживая низкий уровень в клетке. Однако различные клеточные стрессы — повреждение ДНК, гипоксия, активация онкогенов — могут привести к активации p53. После этого он подвергается ряду модификаций (фосфорилирование, ацетилирование и др.), которые стабилизируют и активируют белок.
Активированный p53 действует как фактор транскрипции, связывается со специфическими последовательностями ДНК в промоторных областях своих целевых генов, регулируя экспрессию генов, отвечающих за репарацию ДНК, остановку клеточного цикла, апоптоз и старение. Конкретный ответ зависит от характера и степени повреждений.
В первую очередь p53 останавливает клеточный цикл, но при невозможности восстановления клетка переключается на программу самоуничтожения. Для этого p53 индуцирует синтез проапоптотических белков семейства BCL-2, прежде всего белков-активаторов, которые снимают защиту с митохондрий и активируют белки BAX и BAK. BAX и BAK встраиваются в наружную мембрану митохондрии и формируют поры, через которые цитохром c выходит из митохондрий в цитоплазму. Там он связывается с адаптерным белком Apaf-1, формируя апоптосому, которая активирует каспазу 9. Запускается каскад эффекторных каспаз, и клетка погибает контролируемым образом.
Белок Bcl-XL — один из антиапоптотических белков семейства Bcl-2, локализованный в митохондриях, играет ключевую роль в регуляции апоптоза. Он также взаимодействует с Beclin 1, регулируя аутофагию. Воздействие на Bcl-XL показало потенциальную ценность при аутоиммунных заболеваниях и старении.
Фактор, индуцирующий апоптоз (AIF), — ещё один пример белка, высвобождаемого митохондриями. В отличие от цитохрома c, AIF мигрирует в ядро, где способствует конденсации хроматина и разрыву ДНК, облегчая механизмы клеточной смерти, не зависящие от каспаз. Помимо цитохрома c, AIF и Smac/DIABLO, митохондрии также высвобождают эндонуклеазу G и Omi/HtrA2.
На данном этапе p53 активируется регулярно или постоянно. Он не только останавливает цикл, но и формирует состояние, при котором клетка больше не возвращается к делению. Через повышение экспрессии p21 p53 создаёт первичную блокировку пролиферации. Однако для устойчивой сенесценции одного контура p53/p21 недостаточно. Сенесценция закрепляется вторым путём, через белок p16, который блокирует цикл через ретинобластомный белок. Это делает остановку цикла устойчивым состоянием, сохраняемым даже после исчезновения исходного стимула.
В результате формируется устойчивое сенесцентное состояние — клетка функционально активна, но пролиферативно выключена.
Почему сенесцентная клетка не молчит
Сенесцентная клетка не просто перестаёт делиться, она переходит в состояние, при котором меняется экспрессия множества генов, и формируется секреторный фенотип. Этот фенотип развивается потому, что клетка остаётся метаболически живой и продолжает активно синтезировать белки, но при этом испытывает хронический стресс. Митохондрии работают хуже, накапливаются активные формы кислорода, изменяется состояние хроматина, а элементы повреждённого генетического материала и митохондриальной ДНК могут появляться в цитозоле. Всё это активирует сигнальные пути, запускающие воспалительные транскрипционные программы, прежде всего через NF-kB, а также связанные каскады.
В итоге клетка постоянно выделяет во внеклеточную среду набор молекул: провоспалительные цитокины, хемокины, факторы роста, протеазы и другие компоненты, меняющие поведение окружающих клеток и структуру ткани. Важно, что это не кратковременный сигнал, а хроническая программа, поддерживаемая внутренними положительными обратными связями. Таким образом, сенесцентная клетка становится не просто “остановленной”, а “активно влияющей”.
Внешний контур
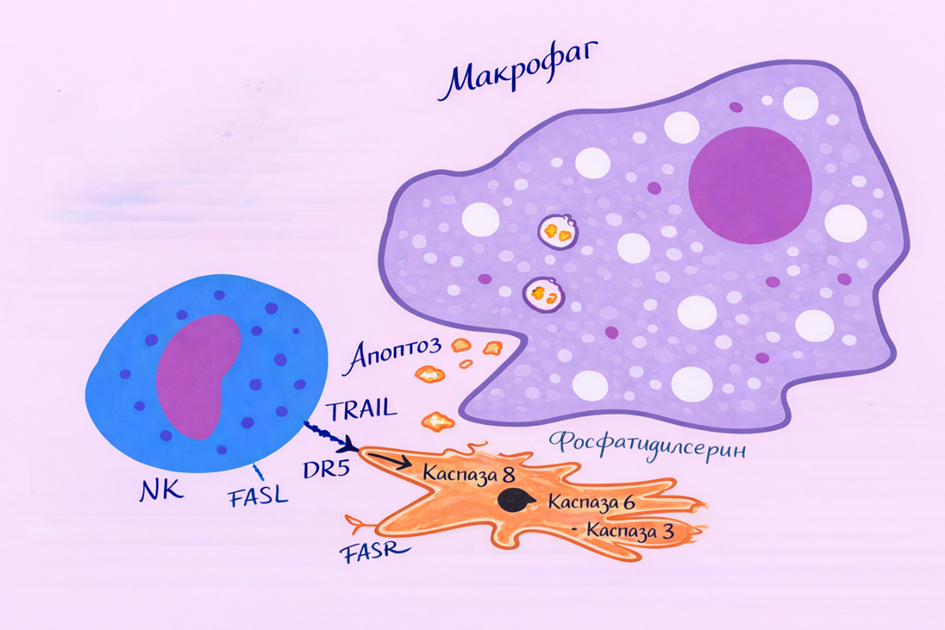
Клетка в состоянии хронического стресса или сенесценции активно меняет своё поведение. Повреждённая или сенесцентная клетка экспрессирует на поверхности стресс-индуцированные молекулы, сигнализирующие иммунным клеткам о ненормальном состоянии. Эти сигналы позволяют натуральным киллерам идентифицировать клетку как потенциально опасную.
Иммунные клетки, получив совокупность сигналов — воспалительный контекст, стресс-лиганды и отсутствие нормального тканевого гомеостаза, — принимают решение об уничтожении клетки. В ответ они экспрессируют или выделяют лиганды рецепторов смерти (Fas-лиганд, TRAIL). Эти молекулы связываются с соответствующими рецепторами смерти на поверхности клетки-мишени, активируя внутриклеточный сигнальный комплекс, в котором запускается каспаза 8. Далее активируется каспазный каскад, и клетка погибает.
Почему иммунитет не убирает сенесцентную клетку сразу?
В условиях старения или хронического воспаления эта система работает неэффективно по двум причинам:
1.Ослабление иммунного надзора. Натуральные киллеры и макрофаги хуже осуществляют фагоцитоз и переваривание, ухудшается архитектура лимфоидных тканей и координация иммунных ответов.
2.Сенесцентная клетка становится устойчивой к уничтожению. Усиливаются антиапоптотические программы, возрастает зависимость от белков семейства BCL-2, блокируются внешние пути апоптоза, повышается порог гибели даже при наличии внешних сигналов смерти. Иммунный сигнал может присутствовать, но клетка оказывается трудной целью.
Влияние воспаления на организм
Воспаление — не исключительно вредный процесс, а фундаментальная защитная реакция организма, необходимая для восстановления тканей и борьбы с инфекцией. Проблема не в самом воспалении, а в его хроническом, неконтролируемом характере.
Что такое воспаление?
Воспаление — естественная реакция иммунной системы на повреждение тканей, инфекцию или воздействие токсинов. Основные признаки (по Цельсу): покраснение, жар, отёк, боль и нарушение функции. Ключевую роль играют цитокины, макрофаги и нейтрофилы, которые координируют очистку очага поражения и запуск заживления. После устранения угрозы воспаление должно завершаться, уступая место процессам восстановления.
Когда воспаление становится опасным?
Если воспаление не завершается, оно становится хроническим, что ведёт к разрушению тканей. Такое «тлеющее» воспаление связано со многими болезнями: атеросклероз, диабет II типа, болезнь Альцгеймера, артрит, онкологические процессы.
Хроническое воспаление часто протекает незаметно, но вызывает повреждения сосудов, нервной ткани и ДНК. Процессы происходят поэтапно, вызывая разрушительные последствия на клеточном уровне.
Постоянная активация иммунных клеток
При хроническом воспалении (в результате инфекции, ожирения, стресса, токсинов и др.) иммунные клетки — макрофаги и лимфоциты — не "выключаются" после борьбы, а продолжают:
·выделять провоспалительные цитокины (IL-1β, TNF-α, IL-6);
·генерировать активные формы кислорода (ROS) и азота (NO), повреждающие ткани.
Эти вещества подобны химическим «осколкам»: они уничтожают микробы, но при длительном воздействии начинают разрушать клетки организма.
Повреждение сосудов
Стенки сосудов постоянно подвергаются воздействию ROS и цитокинов, эндотелиальные клетки теряют эластичность и повреждаются. Организм "латает" повреждения, откладывая липиды и холестерин, что приводит к атеросклерозу:
·образуются атеросклеротические бляшки;
·сосуды сужаются;
·повышается риск инфаркта, инсульта, тромбозов.
Повреждение нервной ткани
Нейроны очень чувствительны к окислительному стрессу. При хроническом воспалении:
·микроглия (иммунные клетки мозга) находится в состоянии постоянной активации;
·выделяются цитокины (особенно IL-1β и TNF-α), мешающие нормальной передаче сигналов;
·накапливаются окисленные белки и липиды, нарушающие работу мембран.
Результат — ухудшение памяти, концентрации, повышенный риск нейродегенерации (болезнь Альцгеймера, Паркинсона), утомляемость, депрессия.
Повреждение ДНК
Активные формы кислорода (ROS), выделяемые при хроническом воспалении, способны:
·ломать цепи ДНК (одно- и двуцепочечные разрывы);
·вызывать мутации;
·нарушать работу генов, отвечающих за деление и репарацию.
Если повреждения происходят в быстро делящихся клетках (например, слизистой кишечника, печени, коже), возрастает риск опухолевых изменений — организм не успевает корректно восстанавливать ДНК.
Почему это незаметно?
Процессы происходят на клеточном уровне и не вызывают острой боли, жара или отёка. В крови может быть лишь слегка повышен С-реактивный белок (СРБ) — маркер воспаления. Человек ощущает усталость, апатию, нарушение сна, "туман в голове", лишний вес, скачки давления — но не связывает это с воспалением.
Факторы, усиливающие воспаление
·Нерациональное питание: избыток сахара, трансжиров, дефицит омега-3 и антиоксидантов.
·Хронический стресс: постоянная выработка кортизола нарушает баланс иммунных реакций.
·Недосыпание: повышает уровень провоспалительных цитокинов (IL-6, TNF-α).
·Малоподвижность: снижает активность противовоспалительных сигнальных путей.
·Ожирение: жировая ткань становится источником воспалительных сигналов.
Как организм регулирует воспаление?
В норме существует тонкий баланс между про- и противовоспалительными молекулами. Основная роль в "торможении" воспаления принадлежит специализированным липидным медиаторам — резолвинам, протектинам и липоксинам, которые "гасят" воспаление после завершения задачи. Недостаток этих веществ (например, из-за нехватки омега-3) мешает завершению воспалительного цикла.
Естественные и медицинские способы регулирования воспаления:
·Питание: больше овощей, фруктов, цельнозерновых продуктов; рыба 2–3 раза в неделю (источник омега-3); ограничение сахара и переработанных продуктов.
·Физическая активность: регулярные умеренные тренировки уменьшают уровень С-реактивного белка и IL-6.
·Сон: не менее 7 часов сна в тёмное время суток.
·Управление стрессом: дыхательные практики, медитация, прогулки, стабильный режим отдыха.
·Медикаменты (по показаниям): НПВС при острых воспалениях.
НПВС — нестероидные противовоспалительные средства
Это группа препаратов, уменьшающих боль, воспаление и температуру, не являясь гормональными средствами (в отличие от кортикостероидов).
Механизм действия: блокируют ферменты циклооксигеназы (ЦОГ-1 и ЦОГ-2), участвующие в образовании простагландинов — веществ, вызывающих воспаление, отёк и боль.
Приём НПВС приводит к уменьшению выработки простагландинов, снижению воспаления и температуры, ослаблению боли.
Примеры популярных НПВС
Кетопрофен
Ацетилсалициловая кислота
Побочные эффекты (важно знать):
·раздражение слизистой желудка (язвы, гастрит);
·риск кровотечений (особенно у пожилых и при приёме аспирина);
·при длительном приёме — нагрузка на почки и печень;
·могут повышать давление у чувствительных людей.
Новый взгляд на воспаление
Цель медицины будущего — не подавлять воспаление, а учить организм правильно его завершать. Изучение молекул-резолвинов и сигнальных путей регенерации открывает новые направления терапии. Воспаление — не враг, а механизм самовосстановления, если работает сбалансированно.
Метрики “воспалительного возраста” (inflammatory age, inflammaging clocks)
Они используются для оценки биологического старения, связанного с воспалением. Основные модели и биомаркеры:
·iAge (inflammatory age) — использует 50 цитокинов, хемокинов и факторов роста, построен с применением глубокого автоэнкодера. MAE — 15,2 года. Главный биомаркер: CXCL9.
·ipAge — основан на 38 цитокинах и хемокинах, использует линейную регрессию. CXCL9 остаётся ключевым маркером, но набор биомаркеров иной.
·SImAge (Systemic Inflammatory Age) — глубокая нейросеть FT-Transformer, требует 10 маркеров, MAE — 6,94 лет. Метод объяснимого ИИ SHAP. Биомаркеры: CXCL9, IL-6, VEGFA, PDGFA, PDGFB, CSF1, IL-27, CXCL10, CCL22, CD40LG.
·CyClo (Cytokine Clock) — LASSO-регрессия, 24 белка иммунной системы крови, MAE — 6 лет. Корреляция с активностью мозговых сетей (МРТ).
·ProtAge — протеомные часы на основе 204 белков плазмы, AI LightGBM-модель, MAE — 4,1 года. Ассоциирован с 18 хроническими заболеваниями и общим риском смертности. Ключевые биомаркеры: CXCL9, GDF15, CXCL17.
·EpInflammAge — эпигенетико-воспалительные часы на основе метилирования ДНК и протеомики, глубокое обучение.
·miRNA-часы — профиль микроРНК (miRNA) крови или кожи. Пока нет строго “воспалительных miRNA-часов”, но микроРНК активно рассматриваются как биомаркеры воспалительного старения.
Ключевые биомаркеры, повторяющиеся в разных моделях:
·CXCL9 — главный универсальный показатель inflammaging: отражает сосудистое и системное воспаление.
·IL-6 — ключевой провоспалительный цитокин, связан со многими хроническими болезнями.
·VEGFA, PDGFA/B — факторы роста, отражающие сосудистую дисфункцию.
·CSF1, IL-27, CXCL10, CCL22 — отражают активацию иммунных клеток и воспалительные каскады.
Смысл этих метрик: “Воспалительные часы” оценивают степень системного воспаления и биологического износа организма. Разница между хронологическим и “воспалительным” возрастом показывает, насколько тело стареет быстрее или медленнее нормы.
Основные биомаркеры воспалительного возраста и их значение
Что важно понимать
·CXCL9 — “звезда” всех моделей. Присутствует почти во всех версиях «воспалительных часов» и напрямую отражает биологический возраст сосудов и эндотелия.
·IL-6, IL-1β, TNF-α — классическая триада «воспалительного старения».
·GDF15 и TGF-β1 — индикаторы общего клеточного стресса, не только воспаления.
·Мультипараметрические модели (SImAge, ProtAge) объединяют 10–200 белков, и по их активности вычисляют «воспалительный возраст» организма.
Ключевая идея: В отличие от обычных «эпигенетических часов» (по ДНК-метилированию), воспалительные метрики отражают состояние иммунной системы, сосудов и межклеточных сигналов — то, что непосредственно связано со старением и риском хронических болезней.
биомаркеров оценивают «воспалительный возраст» организма
16
старения клетки: внутренний (p53) и внешний (иммунный надзор)
2 контура
главный маркер инфламейджинга во всех моделях воспалительных часов
№1 — CXCL9
Другие материалы
Получить первичную оценку документов
Пришлите ваши выписки/снимки/анализы и мы вышлем вам первичную оценку ваших документов






